cho 3,5 gam K2O pahnr ứng vừa đủ với nước (h2O) thu được 4,7 gam KOH. Đưa KOH cho phản ứng hoàn toàn với H2SO4 tạo thành K2SO4 và H2O
a, viết PTHH của phản ứng
b, tính khối lượng nước tham gia
Cho m gam KOH tác dụng vừa đủ với 200g dung dịch H2SO4 9,8% thu được muối K2SO4 và nước. Tính khối lượng KOH đã tham gia phản ứng
\(m_{H_2SO_4}=\dfrac{200\cdot9,8\%}{100\%}=19,6\left(g\right)\\ n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\\ PTHH:2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\\ \Rightarrow n_{KOH}=2n_{H_2SO_4}=0,4\left(mol\right)\\ \Rightarrow m_{KOH}=0,4\cdot\left(39+16+1\right)=22,4\left(g\right)\)
Hấp thụ hoàn toàn m gam SO3 vào nước , thu được 200 g dung dịch H2SO4 19,6%
a,Viết phương trình hóa học của phản ứng . Tính m
b, Lấy 80 gam dung dịch H2SO4 19,6% ở trên cho tác dụng vừa đủ với MgO . Tính khối lượng MgO đã tham gia phản ứng và tính nồng độ phần trăm của dung dịch thu được sau phản ứng
\(n_{H_2SO_4}=\dfrac{200\cdot19.6\%}{98}=0.4\left(mol\right)\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(0.4......................0.4\)
\(m_{SO_3}=0.4\cdot80=32\left(g\right)\)
\(b.\)
\(n_{H_2SO_4}=\dfrac{80\cdot19.6\%}{98}=0.16\left(mol\right)\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(0.16..........0.16..............0.16\)
\(m_{MgO}=0.16\cdot40=6.4\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=6.4+80=86.4\left(g\right)\)
\(C\%MgSO_4=\dfrac{0.16\cdot120}{86.4}\cdot100\%=22.22\%\)
a)
$SO_3 + H_2O \to H_2SO_4$
n SO3 = n H2SO4 = 200.19,6%/98 = 0,4(mol)
=> m = 0,4.80 = 32(gam)
b)
$MgO + H_2SO_4 \to MgSO_4 + H_2O$
n MgSO4 = n MgO = n H2SO4 = 80.19,6%/98 = 0,16(mol)
=> m MgO = 0,16.40 = 6,4(gam)
Sau pư, m dd = 6,4 + 80 = 86,4(gam)
=> C% MgSO4 = 0,16.120/86,4 .100% = 22,22%
cho m gam KOH tác dụng hoàn toàn với 500ml dung dịch HCl dư tạo thành dung dịch KCl 0,15M
a, Viết phương trình phản ứng
b, tính m
c, cho dung dịch KCl trên tác dụng với 2l dung dịch AgNO3 dư 20%so với lượng phản ứng. Tính khối lượng kết tủa thu được và nồng đọ mol các chất có trong dung dịch sau cùng
d, Lọc bỏ kết tủa cô cạn dung dịch thu đc bao nhiêu g muối khan
GIÚP MK VỚI :(
a) PTHH: \(KOH+HCl\rightarrow KCl+H_2O\)
b) Ta có: \(n_{KCl}=0,15\cdot0,5=0,075\left(mol\right)=n_{KOH}\) \(\Rightarrow m_{KOH}=0,075\cdot56=4,2\left(g\right)\)
c) PTHH: \(KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\)
Theo PTHH: \(n_{KCl}=0,075\left(mol\right)=n_{AgNO_3\left(p.ứ\right)}=n_{KNO_3}=n_{AgCl}\)
\(\Rightarrow n_{AgNO_3\left(dư\right)}=0,075\cdot120\%-0,075=0,015\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{AgCl}=0,075\cdot143,5=10,7625\left(g\right)\\C_{M_{KNO_3}}=\dfrac{0,075}{0,5+2}=0,03\left(M\right)\\C_{M_{AgNO_3\left(dư\right)}}=\dfrac{0,015}{2,5}=0,006\left(M\right)\end{matrix}\right.\)
d) Coi như khi cô cạn không bị hao hụt muối
Ta có: \(m_{muối.khan}=m_{KNO_3}+m_{AgNO_3\left(dư\right)}=0,075\cdot101+0,015\cdot170=10,125\left(g\right)\)
Một este X (MX < 200). Lấy 1,22 gam X phản ứng vừa đủ với 100ml dd KOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn cô cạn dung dịch sau phản ứng thu được phần hơi (chỉ có nước) và phần rắn là 2,16 gam muối Y. Đốt cháy hoàn toàn lượng Y thu được 2,64 gam CO2, 0,54 gam H2O, a gam K2CO3. Giá trị của a và tên gọi của X là
A. 1,38 và phenyl fomat.
B. 2,76 và phenyl axetat.
C. 2,4 và phenyl fomat.
D. 1,38 và phenyl axetat.
Đáp án A
Do phần hơi chỉ có H2O nên este có nhóm axit đính trực tiếp vào vòng benzen.
Từ 4 đáp án => là este của phenol ( gốc phenyl).
Như vậy, X sẽ phản ứng với KOH tỉ lệ 1 : 2
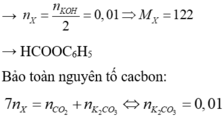
![]()
Cho 3,1 gam Na 2 O phản ứng vừa đủ với nước, thu được 4 gam NaOH. Cho NaOH phản ứng với
H 2 SO 4 , thu được nước và Na 2 SO 4 .
a. Viết các phương trình hoá học của các phản ứng.
b. Tính khối lượng nước tham gia phản ứng.
\(a,PTHH:Na_2O+H_2O\rightarrow2NaOH\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ b,n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\\ \Rightarrow n_{H_2O}=n_{Na_2O}=0,05\left(mol\right)\\ \Rightarrow m_{H_2O}=0,05\cdot18=0,9\left(g\right)\)
nNa2O=3,1/62=0,05(mol)
a) Na2O+H2O->2NaOH
0,05 0,05 mol
2NaOH+H2SO4->Na2SO4+2H2O
nH2O=nNa2O=0,05(mol) =>mH2O=0,05.18= 0,9(g)
Cho m gam Al tác dụng vừa đủ với 300 ml dung dịch CuSO4 1M, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và m1 gam Cu. (a) Viết PTHH xảy ra. (b) Tính khối lượng nhôm (m) đã tham gia phản ứng. (c) Tính khối lượng Cu (m1) sinh ra
Ta có: \(n_{CuSO_4}=0,3\left(mol\right)\)
a, PT: \(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
______0,2____0,3_________________0,3 (mol)
b, \(m_{Al}=0,2.27=5,4\left(g\right)\)
c, \(m_{Cu}=0,3.64=19,2\left(g\right)\)
Bạn tham khảo nhé!
Cho kim loại K phản ứng vừa đủ với 7,2 gam nước, sau phản ứng thu được 18,4 gam kali hidroxit (KOH) và giải phóng 0,4 gam khí hidro H2. Tính khối lượng kim loại kali dã phản ứng.
Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(\Leftrightarrow m_K=m_{KOH}+m_{H_2}-m_{H_2O}=18,4+0,4-7,2=11,6\left(g\right)\)
áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(m_K+7,2=18,4+0,4\)
\(m_K+7,2=18,8\)
\(m_K=18,8-7,2=11,6g\)
vậy khối lượng Kali đã phản ứng là \(11,6g\)
Cho 16 gam NaOH tác dụng vừa đủ với H2SO4 sau phản ứng thu được Na2SO4 và H2O. Tìm khối lượng H2SO4? Tìm khối lượng của Na2SO4 tạo thành sau phản ứng?
PTHH: \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Ta có: \(n_{NaOH}=\dfrac{16}{40}=0,4\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4}=n_{Na_2SO_4}=0,2mol\) \(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4}=0,2\cdot98=19,6\left(g\right)\\m_{Na_2SO_4}=0,2\cdot142=28,4\left(g\right)\end{matrix}\right.\)
nNaOH=m/M=16:40=0.4(mol)
pthh:2NaOH+H2SO4=Na2SO4+2H2O
(mol)0,4 0,2 0,2
mH2SO4=n.M=0,2.98=19,6(g)
mNa2SO4=n.M=0,2.142=28,4(g)
Ở pthh ko viết được mũi tên nên viết bằng dấu bằng nha
Nhiệt phân hoàn toàn 50,59 gam hỗn hợp X gồm hai muối vô cơ MNO3, Al(NO3)3 sau phản ứng thu được chất rắn Y có khối lượng giảm 38,86 gam so với X. Y tan vừa đủ trong 230ml dung dịch NaOH 1M. Đem hỗn hợp X trên phản ứng với dung dịch KOH dư thì lượng KOH tham gia phản ứng là:
A. 0,92 mol.
B. 0,46 mol.
C. 0,94 mol.
D. 0,48 mol.